
آسیه شیرزاد
2 سال پیش
احساس میکنم آخرش کلن همه چی قاتی شد و استاد اشتباه کردن اکسنده کاهنده رو

آسیه شیرزاد
1 سال پیش
@ابراهیم آقاتقی عاره فهمیدم بعدا آدم وقتی یادبگیریم بعد اینو میبینه میفهمه
(1)
غلام درویشی
1 سال پیش
اونی که اکسایش پیدا میکنه درواقع باعث کاهش الکترون های مولکول دیگر میشه بهخاطر همین کاهندس

زهرا صادقی
2 سال پیش
دقیقا در کتاب نوشته o2 نه اتم

ستاره شکوری
1 سال پیش
بله برای اینکه فهمش راحت باشه اینجوری گفتن
(1)

زهرا خدابخشی
2 سال پیش
اینجا استاد میگن که اتمo در صورتی که تو کتاب نوشته شده O2!! نیم واکنشی که نوشتن اشتباه نیست!؟
(1)

آسیه شیرزاد
2 سال پیش
خودشون گفتن که تو کتاب o2نوشته و من فقط برای یادگیری روشش اینجوری نوشتم

مهدی رحیمی
2 سال پیش
سلام استاد از دوبار مثبت شدن روی فهمید که الکترون ازدست داده
reza ahd
2 سال پیش
از نظر من باید از روش عیرب اذک میرفت
مرضیه جعفری
2 سال پیش
ببخشید یه سوال مثلا اگه عدد اکسایش یه اتم منفی دو بوده و شده حالا مثلا منفی یک الان ما می گیم عدد اکسایش افزایش یافته؟

یاسمن ابراهیمی
2 سال پیش
سلام بله

ستاره شکوری
1 سال پیش
عدد اکسایش: کم شه: کاهش زیاد شه:اکسایش

مرضیه جهانگیری
2 سال پیش
سلام میشه گزینه ت را به روشی که استاد حل میکنن توضیح بدید؟ روشی که در پاسخنامه هست را متوجه نشدم.


زینب مقدم

2 سال پیش
سلام تست چنده؟

مرضیه جهانگیری
2 سال پیش
@زینب مقدم تست ۲ (تمرین یاد بگیریم ۱)

مرضیه جهانگیری
2 سال پیش
@زینب مقدم ممنون از توضیحاتتون زینب جان 🌸 متوجه شدم.

زینب مقدم

2 سال پیش
@مرضیه جهانگیری خواهش میکنم😚💚
پوریا زارعی
2 سال پیش
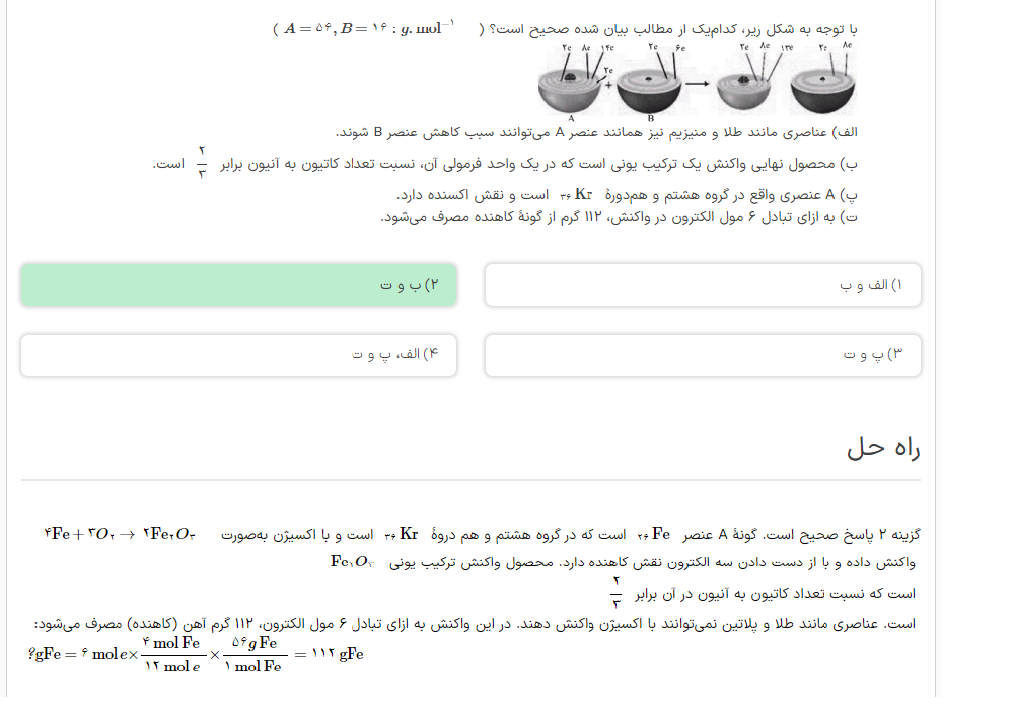
سلام وقت بخیر ببخشید میشه گزینه اخر این تصویر توضیح بدین اون مخرج 12 مول e از کجا اومده؟

آنیا بهشتی
3 سال پیش
سلام.اکسایش و کاهش فقط برای اتم هایی که تو واکنش تشکیل یون میدن(فقط وقتی الکترون واقعا رد و بدل میشه) تعریف میشه؟ یا نه مثل عدد اکسایش وقتی پیوند کووالانسیه و واقعا الکترونی رد و بدل نمیشه هم تعریف میشه؟
(1)

آنیا بهشتی
3 سال پیش
@زینب مقدم پس اون وقت تو توضیح اول صفحه 77 جزوه یا همون اول یادبگیریم 2 یکم ایراد هست.چون گفته طی واکنش های اکسایش کاهش حتما انتقال الکترون از گونه ای به گونه دیگر رخ داده.

آنیا بهشتی
3 سال پیش
@زینب مقدم راستی شما بین مسئول های رفع اشکال هر چهار درس بهترینید:) هم سریع جواب میدید هم توضیح هاتون خیلی کامل هستن قابل فهم هستن.ممنون.
(1)
(1)
(1)

زینب مقدم

3 سال پیش
@آنیا بهشتی ممنوووونم😃 پیامت بهم انگیزه میده✌️🥰
(1)

آنیا بهشتی
3 سال پیش
@زینب مقدم خیلی ممنون توصیحتون عالی بود😍❤

زینب مقدم

3 سال پیش
@آنیا بهشتی خواهش میکنم رفیق جان😃🥰❤️
(1)

محدثه اباذری

3 سال پیش
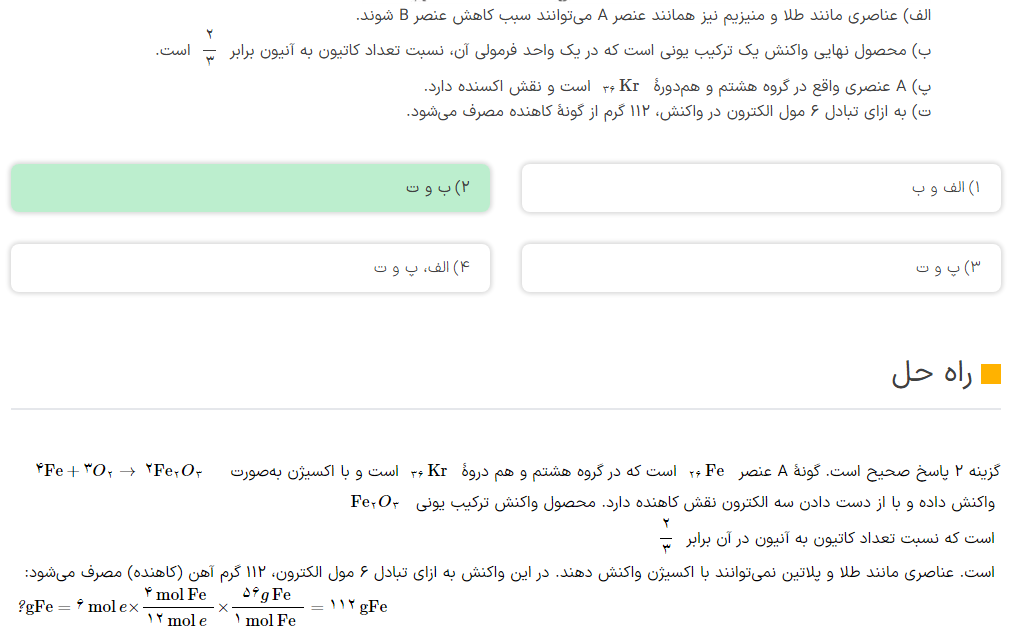
هر مول Fe، سه مول الکترون از دست میده. پس برای مبادله ۶ مول الکترون، ۲ مول Fe مصرف میشه. هر مول Fe پنجاهوشش گرمه. مجموعا میشه ۱۱۲ گرم. ۱۱۲=۵۶×۲

عارف حیدرپور
3 سال پیش
سلام وقت بخیر ببخشید میشه در مورد گزینه های سوال 1 تمرین این قسمت توضیح بدید :) که مثلا از کجا میشه گرماده بودن یا نبودن واکنشمون رو تشخیص بدیم و یا اینکه از کجا فراورذه واکنش رو بفهمیم و در ادامه بفهمیم که حالا کدوم اتم اکسندس یا کاهنده همچنین تاثیر واکنش بر PH محلول...


محدثه اباذری

3 سال پیش
واکنشهای اکسایشکاهش که خود به خود انجام میشن، معمولا گرماده هستن. در خود را بیازمایید صفحه ۴۳ به این موصوع و افزایش دما اشاره شده. در خود را بیازمایید صفحه ۴۲ کتاب، نوشته فلزها (Zn) در واکنش با اسید (HCl)، گاز هیدروژن (H2) و نمک (ZnCl2) تولید میکنن. فرواردهها معلوم شد. قبل از واکنش یه اسید قوی داشتیم (Ph کم) که در واکنش شرکت کرد و بنوعی از بین رفت و Ph به حالت خنثی برگشت. (افزایش ph)

𝒀𝒆𝒈𝒂𝒏𝒆 𝑺𝒂𝒍𝒊𝒎𝒊
3 سال پیش
سلام وقت بخیر.. اونجا که استاد نیم واکنش اکسایش روی و اکسیژن رو نوشتن ، واکنش اکسایش کاملش چی میشه اگه بخوایم درست بنویسیم؟(با O2 درنظر بگیریم)
(1)

محدثه اباذری

3 سال پیش
2Zn+O2->2ZnO
(2)
K .Sh
3 سال پیش
















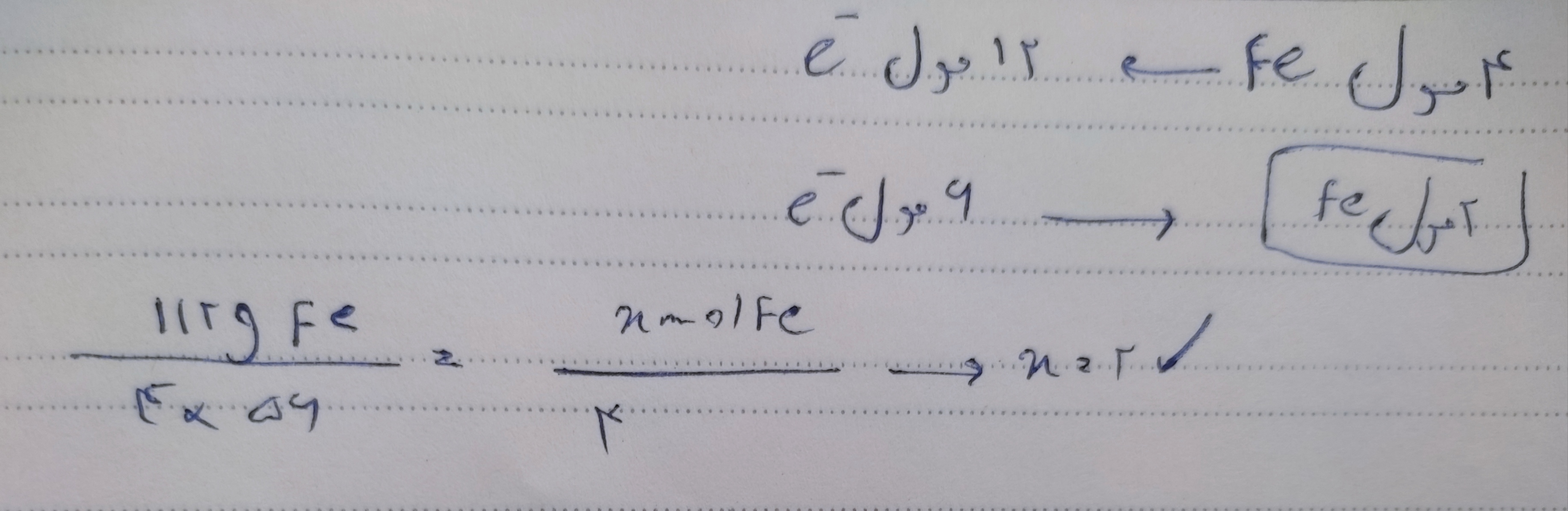

ابراهیم آقاتقی
2 سال پیش
نه اوکی بود استاد مفهومی گفت ولی اگر میخوای یادت بمونه برعکسه یعنی اینکه اونی که اکسایش میابه بر عکسش کن کاهنده است و اونی که کاهش میابه برعکس اکسنده است امیدوارم متوجه شده باشی