سوالات دیگران

فاطمه محمدی
2 ماه پیش
تو این سوال برای بدست اوردن مول غلظت در حجم ضرب ولی تو تستای دیگه برا بدست اوردن مول استاد غلظت رو در حجم تقسیم میکنه
امیر خداوردی
3 ماه پیش
همیشه میشه غلظت نهای هاش مثبت رو در حجم ضرب کنیم جواب بدست بیاد یا شانسی تو این سوال شد ؟

مانی امیری
1 سال پیش
چرا درصد بونش رو بازم تو صد ضرب کرد

سید محمد متین رشادی

1 سال پیش
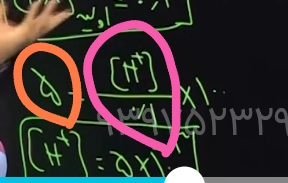
ببین نسبت مولکول های تفکیک شده(که برابر با تعداد هاش مثبت تولید شده هست ) به تعداد کل مولکول های اسید ضعیف،به ما درجه یونش رو میده(رنگ صورتی) حالا درجه یونش ضربدر ۱۰۰،به ما درصد یونش رو میده (رنگ نارنجی)

مرضیه .
1 سال پیش
سلام مگه H+ نمیره میچسبه به آب میشه H³O پس ما نباید اون رو حساب کنیم پس جواب صفر میشه؟؟؟

زینب مقدم

1 سال پیش
سلام منظورش قبل این اتفاقه کلا میخواد ببینه چقد H مثبت و A منفی تولید شده

اسما کریمی
1 سال پیش
چرا مول اولیه این شد؟؟
(1)

زینب مقدم

1 سال پیش
سلام سوال غلظت اولیه رو داده ۰/۱ مول بر لیتر حالا بخوایم مول اولیه رو داشته باشیم باید ضربدر حجمش کنیم که حجم رو هم ۰/۵ داده حالا حاصل ضرب این دو تا میشه ۰/۰۵ اوکیه؟

اسما کریمی
1 سال پیش
@زینب مقدم مرسی

زینب مقدم

2 سال پیش
۲۵ هزارم از کجا اومده؟

مجید دلاکه
2 سال پیش
@زینب مقدم 0/5روبا0/05ضرب کردم

مجید دلاکه
2 سال پیش
@زینب مقدم مرسی عزیز

زینب مقدم

2 سال پیش
@مجید دلاکه خواهش میکنم رفیق جان:)
(1)

مبینا بخشش خدا
2 سال پیش
mishe lotfn tozihe in ravesh ro qarar bedin .

ریحانه قناد
3 سال پیش
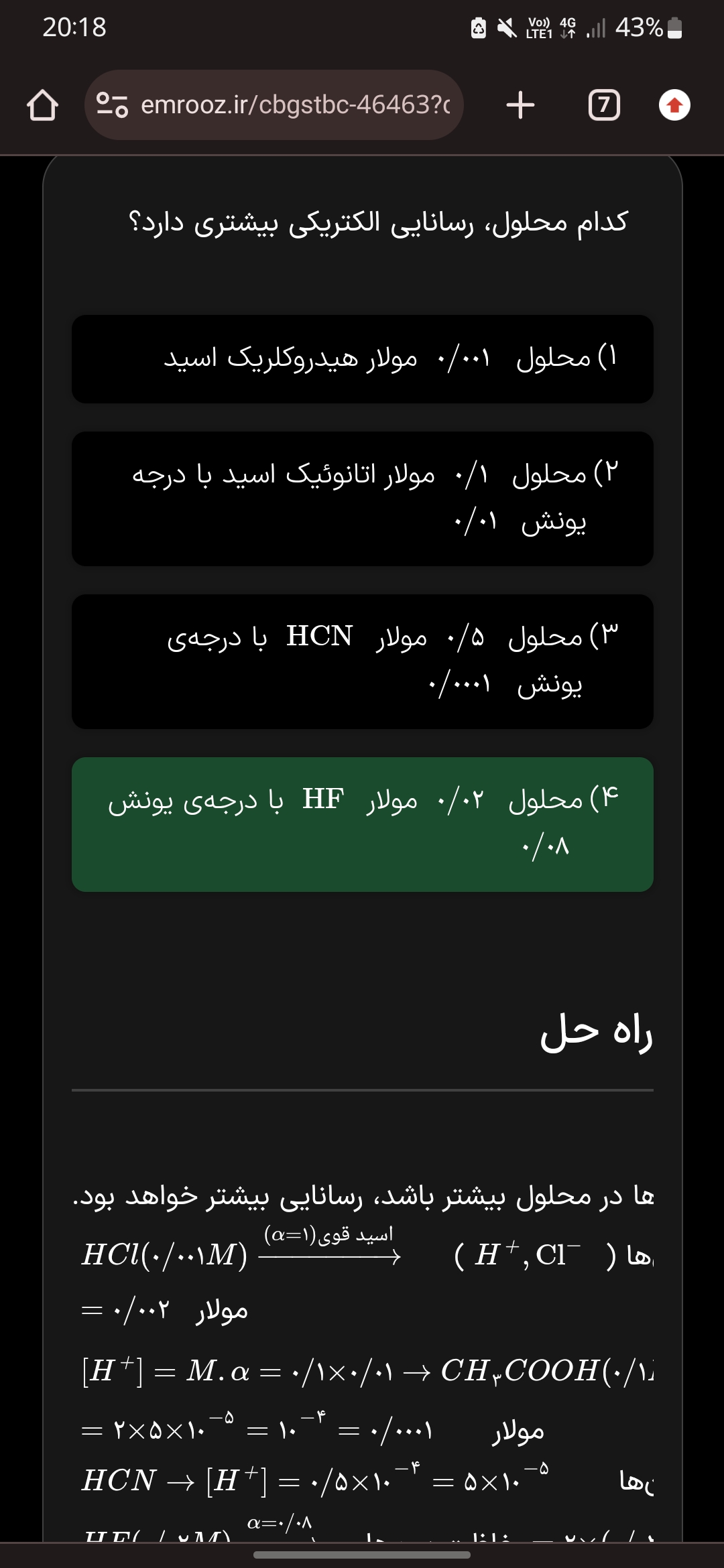
سلام خسته نباشید ببخشید من متوجه نشدم که چرا اینجا استاد پنج صدم منهای بیست و پنج ضربدر ده به توان منفی چهار رو هم در نظر گرفتن لطفا توضیح بدید
(1)

زینب مقدم

3 سال پیش

















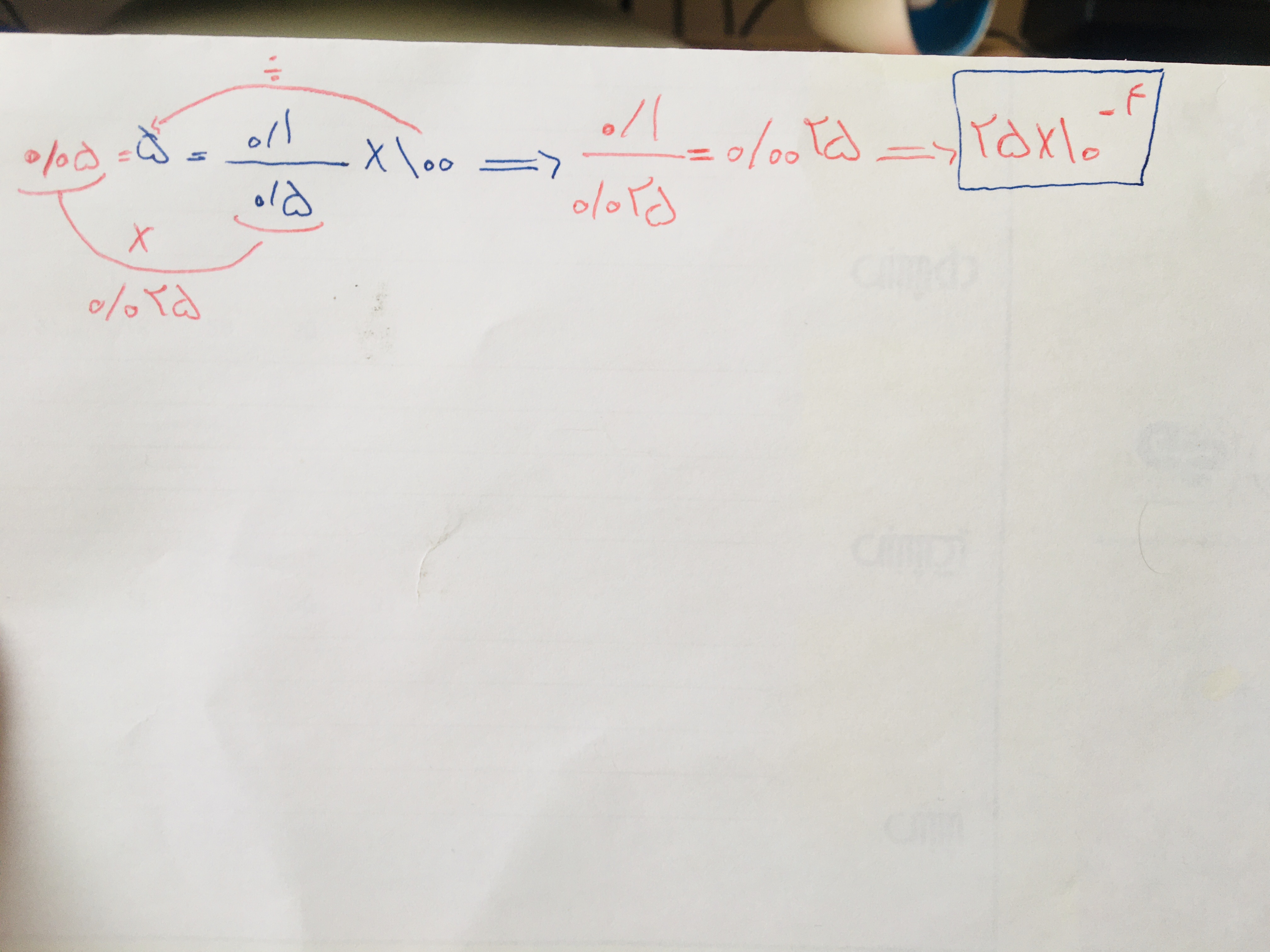



نرگس مهدوی
10 ماه پیش
https://emrooz.ir/cbgstbc-39846?comment_id=465767#comment-465767 اینجا توضیح داده شد