سوالات دیگران

غزل غضنفری
6 ماه پیش
ببخشید من تست های 9 و 10 رو ندارم فیلم شو

سید محمد متین رشادی

6 ماه پیش
بفرمایید https://emrooz.ir/cbgstbc-64568 https://emrooz.ir/cbgstbc-64569

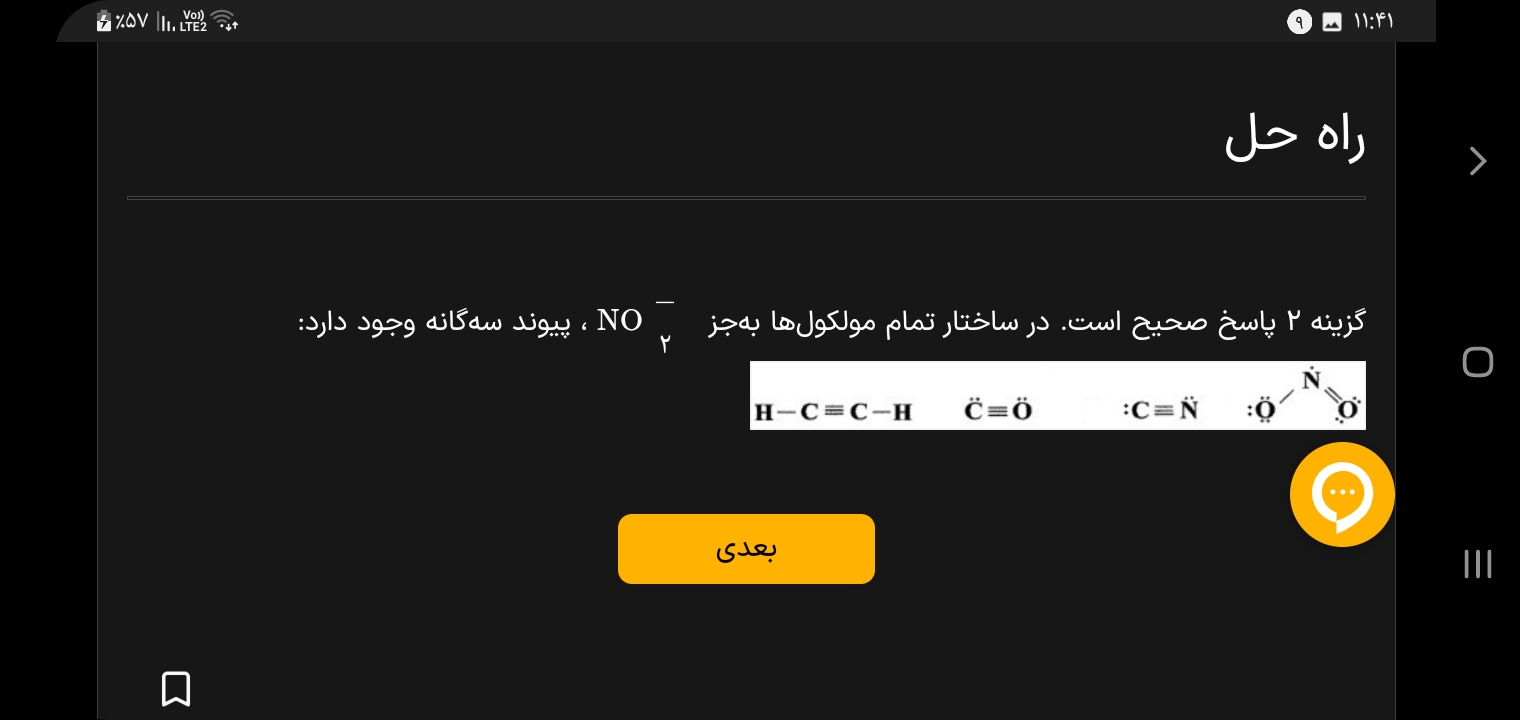
👩🏻⚕️ 🩺
1 سال پیش
در هر پیوند داتیو چند الکترون به اشتراک گذاشته میشود؟؟ بعد از پیوند داتیو اکسیژن ۶ تا الکترون ناپیوندی داره؟

سید محمد متین رشادی

1 سال پیش
در هر پیوند داتیو،یکی از اتم ها،لطف میکنه و به تنهایی دوتا الکترون به اشتراک میذاره ولی نمیدونم در چه مولکولی منظورتون هست

👩🏻⚕️ 🩺
1 سال پیش
@سید محمد متین رشادی ب فرض مثال اگه اکسیژن یه پیوند داتیو داشته باشع

امیر محمد رضایی
1 سال پیش
من که شیمی رو میخوردم الان بخدا با این توضیحات بد تر داره یادم میره چرا من اینجوری شدم😐💔
(1)

سید محمد متین رشادی

1 سال پیش
بنظرم بطور کلی خوب توضیح میدن ولی باز اگر جایی رو یکم دست بالا توضیح دادن و متوجه نشدی،سوال کن جواب میدم💙💙
مینا علی عباسی
1 سال پیش
دقییییییقا منم همینم با شیمی🤦🏼♀️
امیر محمد حسنیان
1 سال پیش
اونجایی که استاد که استاد گزینه سه رو جواب در نظر نگرفتن برام سواله که، گفته آرایش هشت تایی پایدار، ولی کربن مونو اکسید ناپایداره و در اکسیژن کافی به سی او دو تبدیل میشه،پس چرا صحیح گرفتن؟

سید محمد متین رشادی

1 سال پیش
نه کربن منوکسید که به کربن دی اکسید تبدیل نمیشه خودش یه مولکول پایداره ولی خیلی سمی هست و مایل به واکنش...
(1)

NAFAS
1 سال پیش
برای گزینه 3 اونجایی که استاد میگن ساختار های خاص یا اونایی که هیدروژن دارند به دوتایی رسیدن رو میشه توضیح بدید منظور از دوتایی چیه؟

نرگس مهدوی

1 سال پیش
سلام ما میگیم برای به پیادارب رسیدن اتم ها باید ارایش هشت تایی پیدا کنن اما توی هیدروژن اینطوری نیست دیگه وقتی دو تا الکترون بگیره پایدار میشه برای همین یه پیوند تشکیل میده فقط

مریم خدایی
1 سال پیش
من ج رو متوجه نشدم ی توضیحی میدین؟

سید محمد متین رشادی

1 سال پیش
در مورد فسفر ترس کلرید،دقیقا چیش رو نفهمیدید؟ تعداد الکترون های ظرفیت یا ساختارش یا...؟

مریم خدایی
1 سال پیش
@سید محمد متین رشادی هم الکترون های ظرفیت و هم اینکه چجور شد به هشت تایی پایدار رسیدند/

سید محمد متین رشادی

1 سال پیش
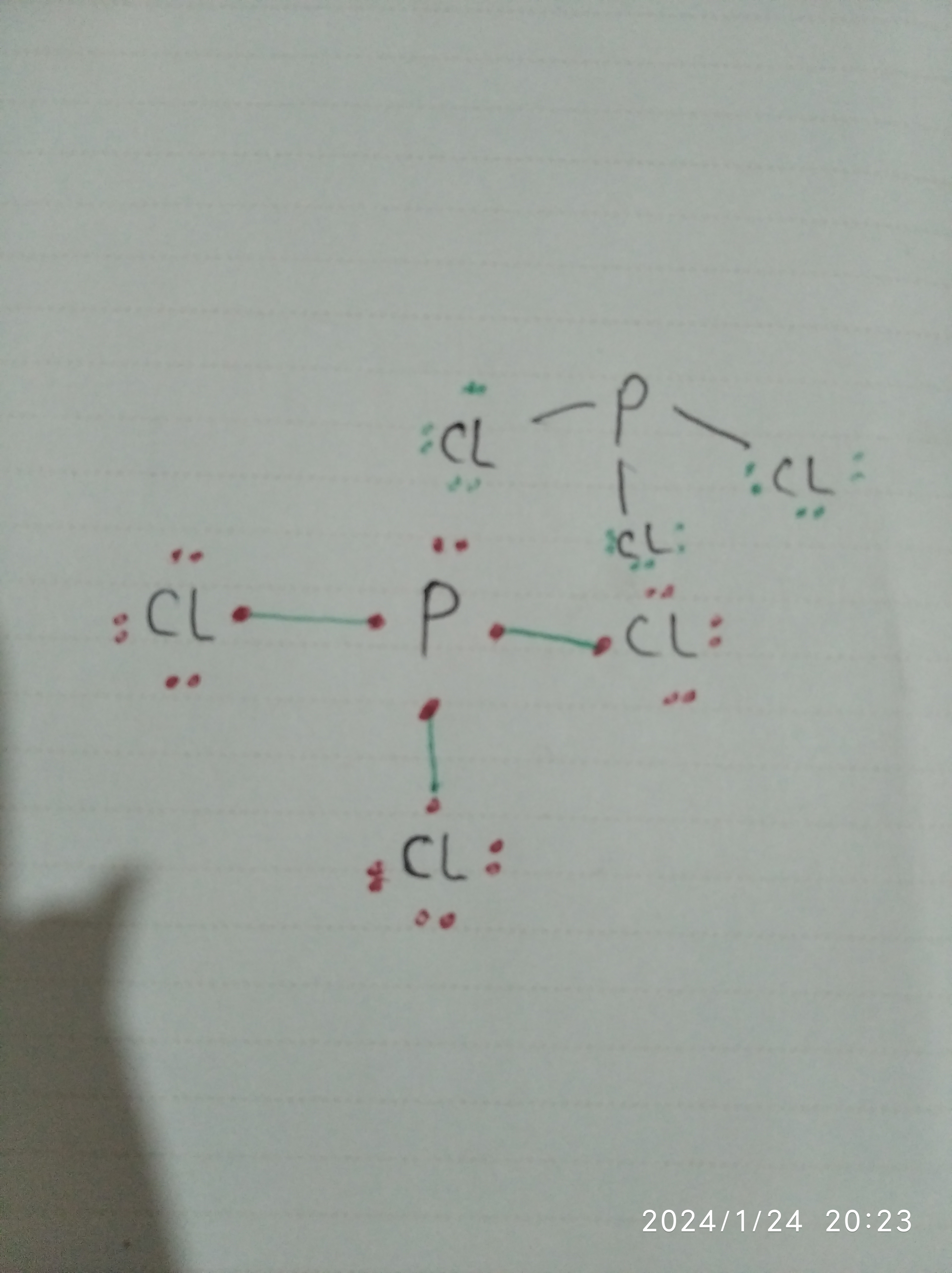
@مریم خدایی ببینید فسفر پنج تا در لایه ظرفیتش داره و سه تا کم داره تا به هشت تایی برسه پس سه تا الکترون باید بذاره وسط تا به ازای هر کدوم هم،یه اتم دیگه یه الکترون بیاره بذاره وسط مشترکا استفاده کنند تا فسفر هشت تایی بشه اونایی که میان با فسفر پیوند میدن توی این ترکیب،کلر هستن هر کلر یک الکترون با فسفر به اشتراک میذاره و یک پیوند اشتراکی میده و خودش هم هشت تایی میشه(چون هفت تا داره در لایه ظرفیتش) حله؟

مبینا اشراقی
2 سال پیش
سلام خسته نباشید میشه ساختار لوییس فسفر تری کلرید رو رسم کنین و توضیح بدین

جمیله شهنوازی
2 سال پیش
سلام استاد گفتند تو ساختار لوویس میای اتم مرکزی که دارای بیشترین الکترون تنهاست رو انتخاب میکنی خب ببین فسفر گروه 15 الکترون های تکش میش 3تا خب و کلر گروه 17 الکترون های تکش میش 1 دونه خب پس فسفر انتخاب میکنیم eتک ۳ تا داره بعد میای بقیه اتم های کلرو ب اتم مرکزی وصل میکنی

جمیله شهنوازی
2 سال پیش
کافیه فرمول نویسی و جدول تناوبی بلد باشی با توضیحات استاد خیلی دیگ راحت تست هاش آسون میش برات 🙃🌷

مریم سادات موسوی
2 سال پیش















زینب مقدم
5 ماه پیش
اره جزئیات زیاد داره