سوالات دیگران

محمدجواد ظهیری اصل
7 ماه پیش
سلام میتونیم مول منیزیم هیدروکسید و آلومینیوم هیدروکسید رو حساب کنیم بعد فرمول واکنش خنثی شدن رو بنویسیم؟

محمدحسین ولیزاده
1 سال پیش
سلام چرا وقتی میتونیم ph دقیق رو بدست بیاریم از ما تقریبی میگین حساب کنیم به نظرم این سوالات ایراد دارن لطفا رسیدگی کنین خود استاد هم گفت این حرفو


سید محمد متین رشادی

1 سال پیش
سلام بله درسته اینجا نباید بگه حدودا ولی دقیقش رو حساب کنیم میشه ۷/۳ که اصولاً باید بذار توی گزینه ها ولی حالا که نذاشته،ما اگه سر امتحان باشیم،اونی رو میزنیم که بهش نزدیک تره (چون گفته حدودا)

علیرضا سهرابی
2 سال پیش
سلام لطفا به روش M1.V1.X1=M2.V2.X2 + M3.V3.X3 برام حل کنید
(1)
(4)

.... .....
2 سال پیش
@maryam chaghaei چه خط باحالی داری رفیق! D:
(3)

maryam chaghaei
2 سال پیش
@.... ..... لطف داری😅
(1)

مرتضی مرتضوی
2 سال پیش
سوال اش خیلی قشنگه وترکیبی بنظرم خیلی احتمال اش زیاده دوباره مطرح اش بشه یکمی باایده خلاقانه تر.چون کنکور بیشتر به این سمت داره میره
(2)
پوریا زارعی
2 سال پیش
سلام وقت بخیر ببخشید من از M1.V1.X1=M2.V2.X2 + M3.V3.X3 رفتم از این هم درسته؟
(1)

حنانه یارمحمدی
3 سال پیش
سلام وقت بخیر توتمرین ها تمرین ۱۰ میشه بهم توضیح بدین اصلا متوجه نمیشم🙏🏻
نسیم جاودانی

3 سال پیش
سلام منظورتون کدوم تمرین ۱۰ هست؟

حنانه یارمحمدی
3 سال پیش
@نسیم جاودانی تمرین یاد بگیریم که اخر تست ها قرار داده شده

رعنا نجات
3 سال پیش
استاد چرا مول HCl رو محاسبه کردن در صورتی که سوال نمیخواستش؟
نسیم جاودانی

3 سال پیش
سلام دوست عزیز شیره ی معده همون HCl هست

امیرحسین زارعی
3 سال پیش
سلام ببخشید سوال ۶ تمرین قسمت دومش و اینکه چطور نتیجه گرفت محلول خنثی هستش رو میشه توضیح بدید
(1)
(1)

کوثر معتقد
3 سال پیش
سلام میشه سوال 10 تمرین یادبگیریم همین قسمتو توضیح بدین

محدثه اباذری

3 سال پیش
اول باید از Ph محلول HA، غلظت H+ رو پیدا کنیم. باتوجه به اینکه گفته غلظت یون هیدرونیوم محلول بازی HOB، ۲/۵ ضربدر ۱۰ بتوان ۵- برابر غلظت یون هیدرونیوم در محلول اسیدی AH هست، غلظت یون هیدرونیوم محلول BOH رو محاسبه میکنیم. وقتی BOH در آب حل شه، OH- آزاد میکنه، پس باتوجه به قاعده H+][OH-]] مساویست با ۱۰ بتوان ۱۴-، غلظت OH- رو حساب میکنیم. درجه یونش BOH یکدهمه. یعنی یکدهم BOH حلشده یونیده شده و OH- آزاد کرده. باتوجه به ایننکته، غلظت BOH رو حساب میکنیم. بعد هم با کسر زیر، مقدار HBr رو حساب میکنیم.
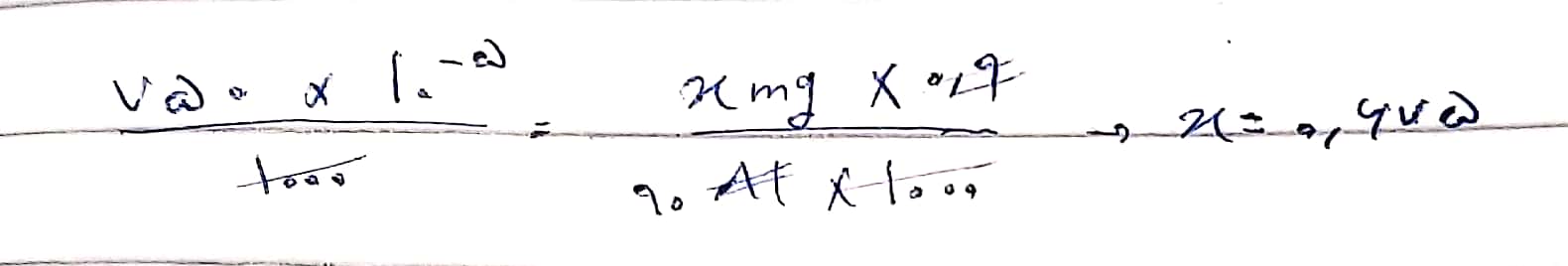














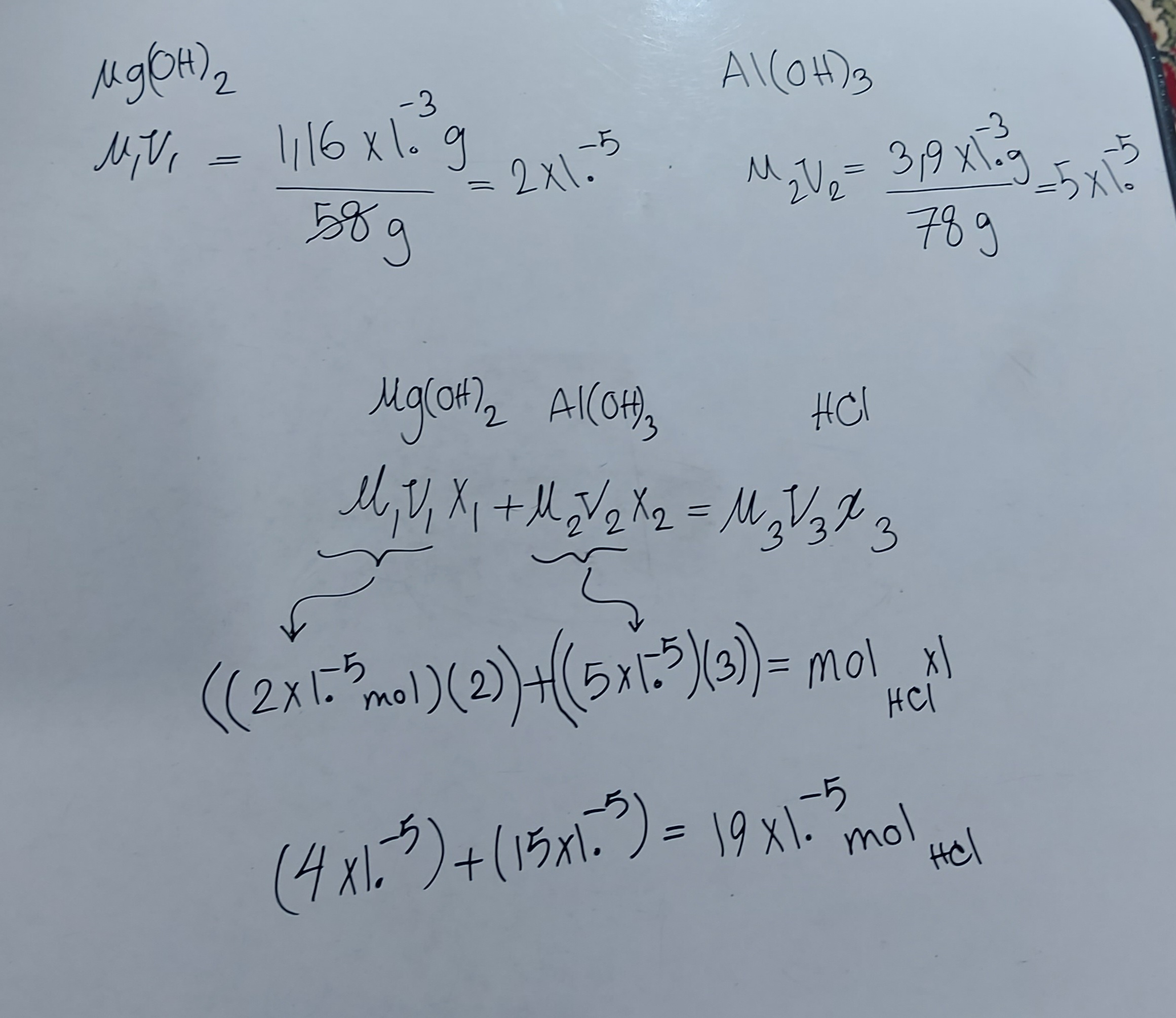

نرگس مهدوی
1 سال پیش
سلام از واکنش دوم بدستش اوردیم یعنی گفتیم که فرد ۳.۹ میلی گرم الومینیوم هیدروکسید مصرف میکنه، پس این الومنیوم هیدروکسید چقدر هیدروکلریدریک اسید رو خنثی میکنه؟ میشه ۱۵ ضربدر ۱۰ به توان منفی ۱۵ مول Hcl